こんにちは、まるこです。
2020年の診療報酬改定で、「早期栄養介入管理加算」が新設されました。
今後もっと管理栄養士が注目を浴びる日がくるのかな、と思うと嬉しくなります。
私もガンバラネバ(- -;)
すでに新設されて3年が経とうとしており、だいぶ遅れをとってしまいましたが、今回は勉強も兼ねて早期栄養介入加算関連の栄養管理をまとめてみました。
参考にしたのが、日本集中治療医学会「日本版重症患者の栄養療法ガイドライン」。
2016年に「総論」、2017年に「病態別栄養療法」が示されており、内容はネットでも閲覧できます。
長くなるので今回は、「総論」の内容。
個人が勝手にまとめた記事になりますので、直接業務で関わる場合は、日本集中治療医学会「日本版重症患者の栄養療法ガイドライン」を参照されることをお勧めします。本記事は参考程度でお願いします。
重症患者
ここでいう重症患者は、敗血症、重症外傷、外科手術後、重症熱傷、肝不全、急性膵炎など、循環管理、呼吸管理をふくめた集中治療を必要とするもの


重症患者の代謝の特徴
重症患者の代謝は、一般的な栄養障害の飢餓の時とは異なります。
飢餓時は食事からのエネルギー供給がないので、脂肪組織や筋蛋白を分解(異化亢進)してエネルギーを得ます。この場合食事をすると異化亢進は止まります。
対して重症患者。急性侵襲を受けているときは、ストレスホルモン、サイトカインなどの炎症性メディエーターが上昇し、筋蛋白の分解が進みます(異化亢進)。この場合、食事を摂取しても原疾患が治らない限り異化亢進は止まらない。つまり、外因性エネルギー(わたしたちの行う栄養療法)をうまく利用できなくなります。
侵襲時は異化亢進する上にエネルギー・蛋白の需要は高まるので、容易に栄養不足に。
内因性エネルギー:異化によって得られるエネルギー(グリコーゲン・脂肪・筋蛋白を分解)
外因性エネルギー:私たちが行う栄養療法
注意したいのが、重症患者の過剰栄養(overfeeding)!
消費エネルギー増大を考慮してエネルギー投与量を増やしても、異化亢進(内因性エネルギーの増大)は避けられません。そのあたりを踏まえてエネルギー投与量を調整しないと、エネルギー供給量過剰になります。
重症患者ではoverfeedingになりやすく、感染症合併症の増加、死亡率の上昇につながります。
一方で、エネルギー消費量が摂取量を上回る状態(underfeeding)が長期化すると、入院期間の延長や死亡率の増加に繋がるといわれます。
栄養リスク評価
重症患者において信憑性の高い評価方法はないので、SGAや病歴、入院前の食事摂取、体重、重症度スコア(qSOFAなど)をもとに総合的に評価します。
- 体重や身体計測値(皮下脂肪・筋肉量など):輸液や体液変動に影響される
- アルブミンなどの血清蛋白:炎症反応や血管透過性亢進による血管外漏出に影響される
栄養投与ルート
▶栄養投与ルートは経腸栄養を優先する。
経管栄養優先が推奨される根拠
- 経腸栄養は、感染症発症率、入院日数において有利。※死亡率は有意差なし
- 重症患者に対する早期の経腸栄養は、感染合併症リスク軽減。
早期の経腸栄養は、
- 腸管粘膜萎縮、粘膜バリア破綻を予防
- 正常な腸管細菌の保持
- 消化管生理機能の維持
- Bacterial translocationの回避
といった、腸管機能を保ち吸収能を改善させる効果があります。
その他ENのメリットとして、ある程度吸収量の調整が可能となるのでoverfeedingを回避しやすいこと(インスリン必要性も静脈栄養より低下)や、輸液(PPN・TPN製剤)より経腸栄養剤のほうがコストを抑えられて経済的なことがあげられます。
 まるこ
まるこ侵襲後は消化管運動が低下するので、開始が遅れるほど経腸栄養の管理が大変に!
a 経腸栄養
経腸栄養の開始時期
▶経腸栄養は、ICU入室後可及的に24時間以内に、遅くても48時間以内に開始。
消化管に問題がなく、循環動態が安定していれば早期に経腸栄養を開始!
腸管蠕動の有無は経腸栄養開始の判断基準にはならない
ガイドラインでは、腸管蠕動の確認を経腸栄養開始の条件としないことを強く推奨しています。経腸栄養そのものが腸管運動を促進するといわれます。
以下、ガイドラインを参考に記載。
- 腸蠕動音、排便・排ガスの確認が取れなくても、ICU入室48時間以内に早期経腸栄養を安全に開始することが可能であると報告されている(ただし、これらの対象の多くが外科術後患者である点を考慮する必要がある。)
- ICU 症例や術後の消化管機能不全の要因は、①粘膜バリア層の破綻、②蠕動低下と粘膜層の萎縮、③腸管関連リンパ組織(GALT)容量の減少に3つに分類される
- 一般に経腸栄養開始の基準となる腸管蠕動音は,腸管運動を知る唯一のサインではあるが,蠕動音は腸管のバリア機能、吸収能を示すサインではない
- 患者の血行動態が安定している限り,軽度〜中等度のイレウスに対して経腸栄養を投与しても安全であり適正である
経腸栄養が難しい病態
腸管虚血・腸管壊死のリスクが高い病態、大量の心血管作動薬剤を必要とする病態での経腸栄養は難しいです。明らかに経腸栄養を遅らせた方が良い病態は、
- 経腸栄養の禁忌(腸閉塞(通過障害)、活動性の消化管出血、明らかな腸管虚血など)
- コントロールできていないショック
- 不安定な循環状態 ☜☜☜



その他経腸栄養の禁忌とは、難治性嘔吐や重篤な下痢、汎発性腹膜炎、短腸症候群、炎症性腸疾患(急性期)、腸管壊死 。。など
「不安定な循環動態」とは?
不安定な循環動態とは、高容量の心血管作動薬投与、大量輸液・輸血が必要な病態。
心血管作動薬
ドパミン(イノバン)、ドブダミン(ドブポン)、アドレナリン(ボスミン)、ノルアドレナリン、バソプレシン(ピトレシン) など
循環動態が安定してきた目安(経腸栄養開始を検討する目安)
平均血圧60mmHg以上、心血管作動薬の増量がない、大量輸液・輸血の必要がない
平均血圧(MAP)
平均血圧は、常に動脈にかかっている圧力の平均的な値。臓器還流の指標で、臓器血流を実質的に規定している。
平均血圧=脈圧(収縮期血圧 -拡張期血圧)÷3 +拡張期血圧。正常値は90未満とされる。
平均血圧が高いと末梢の細い血管の動脈硬化が疑われ、平均血圧が60を下回ると脳血流量も急激に低下している。
不安定な状態での経腸栄養リスク
- 腸管血流が低下しているため、経腸栄養により腸管酸素消費量が増大すると、血圧低下や非閉塞性腸管壊死(NOMI)をきたす恐れがある
- 開始後、腸管虚血の症状(経腸栄養開始後の血圧低下、腹部膨満、胃残増加、胃管逆流増加、蠕動音減少、乳酸アシドーシス)を認めた場合は、経腸栄養中止する
チューブの位置
- 誤嚥のリスクがある症例では、幽門後からの経腸栄養を考慮することを弱く推奨。
- 幽門後は肺炎が少ない幽門後にこだわるとENの開始が遅くなる。
- EDチューブ挿入にこだわると経腸栄養開始が遅れることが指摘されている。幽門後投与よりENの早期開始を優先することを考慮すべき。
- 挿入方法は内視鏡ないし造影下で。
誤嚥の高リスク
鎮静中、筋弛緩薬使用中などの重症患者。頭部挙上ができない患者で胃残量が多い場合など
経腸栄養耐性のモニタリング方法
- 患者の経腸栄養に対する耐性(継続できるか?)として、疼痛や腹部膨満感の訴え、理学所見、排ガス・排便、腹部X線写真などをモニタリングする。
- 不耐性を示す他の徴候がない場合,随時確認した胃内残量<500 mlであれば経腸栄養を中断しない。経腸栄養の不適切な中止を避ける。



ガイドラインでは、経腸栄養増量するにあたり次のことを定めたプロトコールを作成するようにとあります。
①目標注入速度の設定、②より早期の経腸栄養開始法、③胃内残量、④チューブフラッシュの頻度、⑤栄養投与を調節・中止する状態、⑥合併症の取り扱いに関する指示
ICUスタッフが運用するプロトコールを使用することで、投与される目標量の達成度が上昇します。
b 静脈栄養
静脈栄養の開始時期
まず、静脈栄養は積極的には行わないのが原則!
最初の1週間に経腸栄養が20kcal/hr以上(480kcal/日以上)投与できれば、目標量達成を目的とした静脈栄養は行わないことを弱く推奨しています。
memo✎
- ENで20kcal/hr未満の場合は、PN併用(SPN)が良いか
- ペプタメンAFでENを開始する場合:1本200ml(300kcal、蛋白19g)なので、24時間持続投与だと1時間あたり8.3ml(12.5kcal、蛋白0.8g)になる。1日2本に増やせればSPN不要
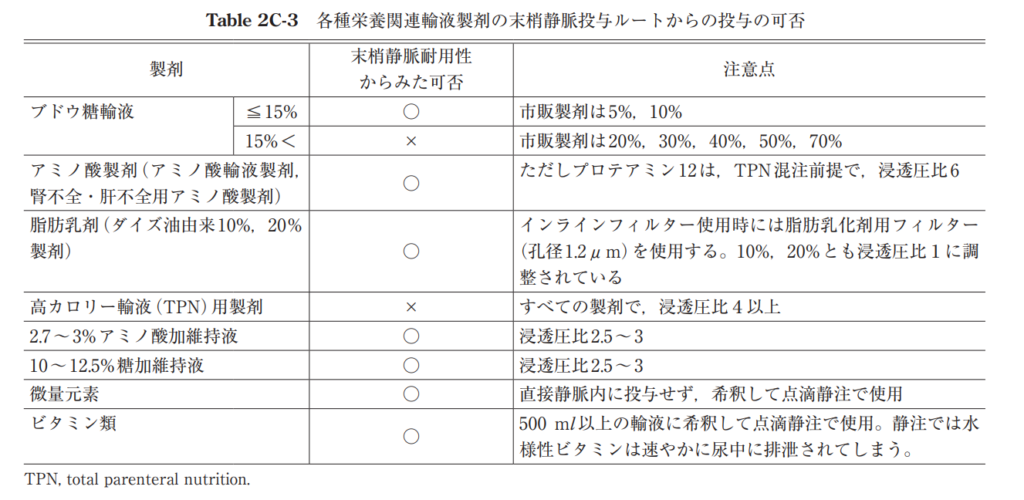
- ブドウ糖輸液単独では行わないことを弱く推奨
- 重症度の高い集中治療患者への総合ビタミン剤、微量元素製剤の通常量の投与を強く推奨



中心静脈用の微量元素製剤はセレンが含まれていません。そのため、セレン欠乏症に注意。
日本で経静脈的投与のセレン製剤も市販されていないため、経静脈投与をする場合は施設における製剤(亜セレン酸ナトリウム)の作成とIRBの承認などが必要、一般的な投与方法は未だないそうです。

エネルギー投与量
▶簡易式25~30kcal/体重kgを用いる
エネルギー消費量は間接熱量計の結果、もしくは推算式による算出に基づいて設定することを強く推奨しています。
Harris-Benedictの式は欧米人のデータから作られたもので、重症患者では過剰栄養となる可能性があります。
そのため、ひとまず簡易式を用いて計算するのがよさそう。
memo✎
- PN単独では、3~7日以内に開始し、ICU入室7日目までに簡易式20~25kcal/体重kgを目標。(ガイドラインではPNの開始時期や至適エネルギー投与量は明確ではない)
Permissive underfeeding
▶重症患者には、最初の1週間は消費エネルギーよりも少なく投与することが望ましいとされます。
▶EN+PNでは、栄養開始3~7日で簡易式(25~30kcal/体重kg)の70%程度(未満)が目標。
memo✎
- 簡易式25~30kcal/体重kg×70%=17.5~21kcal/体重kg なので、最初の1週間はだいたいEN+PNで20kcal/体重kgを目指すのが良いか
- PN単独では簡易式20~25kcal/体重kgの70%程度(未満)が目標
- 栄養開始後4~7日目を目安に投与量を漸増する
蛋白質投与量
▶蛋白質は1.0〜1.2 g/体重kg以上(ガイドライン上での提案)
▶各国のガイドラインも加味すると、1.2 g/体重kg以上がよいか
- エネルギー投与量が目標量に達している場合は、1.2〜2.0 g/(実測体重)kg/dayの蛋白が喪失している
- 腎代替療法施行中の患者では、透析膜からの蛋白喪失量を勘案して1.5g/体重kg/dayの高めの目標設定が推奨される
- タンパク質より多く投与することで死亡率を低下させる研究結果もある(ICU入室4日目までに1.2g/体重kg以上)
血糖コントロールの重要性
▶目標血糖値は180mg/dL以下
重症患者の栄養が適正かどうか、血糖値をみて評価できます。
- 急性侵襲時はストレスホルモンが分泌されてインスリン抵抗性が増大し、高血糖になりやすい
- 重症患者は貧血であることが多く簡易血糖測定器では血糖値は高めに表示されるので血液ガスで測定する
リフィーディング症候群
高齢者、癌患者、アルコール依存症など、慢性的な低栄養患者が急に栄養を摂取することで発症します。水・電解質分布の異常(著しい低リン血症、低カリウム血症)、心合併症(不整脈、心不全)を引き起こす病態。
発症のしくみ
急激な栄養投与がインスリン分泌を刺激し、ビタミンB1や、P・Mg・Kなどのミネラルが急激に細胞内に取り込まれ、消費される。
低リン血症、低カリウム血症
心合併症(不整脈、心不全)、呼吸不全、意識障害
予防・対策
Pなど適切な電解質、ビタミン補正と、少量からの栄養投与。
疑われる場合は、P・Mg・Kのモニタリング。
誤嚥・下痢への対処
誤嚥
- 気管挿管患者では上半身を30~45度挙上する
- 誤嚥ハイリスク患者・経胃投与に不耐性(行うことが困難)を示す患者に対しては、以下を推奨。持続投与や幽門後経路(経空腸投与)への変更、腸管運動促進薬(メトクロプラミドやエリスロマイシン)や麻薬拮抗薬(ナロキソン)を使用
誤嚥ハイリスク患者・経胃投与に不耐性(行うことが困難)を示す患者
①経鼻栄養チューブの使用、②気管チューブと人工呼吸、③年齢>70歳、④意識レベルの低下、⑤看護ケアの不足、⑥入院している病棟(ICUかどうか)、⑦患者の体位、⑧ICUからの移送、⑨口腔ケアの不足、⑩栄養剤の間欠投与 など
下痢
下痢が発生したときは抗菌薬投与に伴う菌交代現象(偽膜性腸炎、MRSA腸炎)に注意!
その他の下痢の危険因子
発熱あるいは低体温、感染巣の存在、低栄養・低アルブミン血症、敗血症、多臓器不全、完全静脈栄養 など
下痢に伴う問題
- 循環血液量の減少
- 代謝性アシドーシス(大量の消化液の排泄による電解質(K・Mg・Znなど)や重炭酸イオンの喪失による)
- 手術創や褥瘡などの汚染
下痢への対策
- 経腸栄養の投与量や投与時間の調節
- 腸管蠕動に関与する薬剤の調整
- 経腸栄養剤の変更(水溶性食物繊維、ペプチド、半固形化、炭水化物と脂肪の含有量(高脂肪低炭水化物×)、高浸透圧など栄養剤の組成) ※食物繊維は腸管虚血に注意。
栄養成分の吸収不良により合併症も増加するため、静脈栄養による補助が必要となることも。
memo✎
- 水溶性食物繊維(ペクチンやグアーガムなど)に比べて不溶性食物繊維は下痢を予防する効果が低い
- 水溶性食物繊維は消化管内容物の粘性を高める効果があり、胃からの排泄や小腸での吸収を遅らせ、腸管蠕動に対する抵抗によって消化管内容物の流れを減弱させる
■プロバイオティクス/プレバイオティクス/シンバイオティクス
腸内細菌叢が保たれ、感染症合併症(腸炎、肺炎、菌血症)減少する効果があるといわれます。ガイドラインでは使用を弱く推奨していますが、プレバイオティクス製剤の種類とプロバイオティクスの菌種が異なるため現状ではまだ確立したものはないそうです。
その他
特殊栄養素
n-3系脂肪酸(ARDS、敗血症)〇、アルギニン×、グルタミン(熱傷〇、ショック・多臓器不全×)、不溶性食物繊維×
米国では消化態栄養剤を推奨していますが、日本版のガイドラインでは有効性を認めていません。
消化管出血
消化管出血リスク高い場合は、胃酸を抑える薬(PPI、H2RA)。
消化管出血リスク低い場合は、スクラルファートなど。
PPIやH2RAは肺炎の発生リスクを上昇させる可能性があるのでリスクを評価し適切に使用。



まとめです。
禁忌がなければ早期に経腸栄養を始める。栄養剤は少量からはじめて、開始1週間は必要量充足を焦らない。特殊栄養素を考えるより、まずはエネルギー量とタンパク質のふたつを考える。血糖コントロールと胃内残量、消化器症状をしっかりモニタリングしていく。
参考にさせていただきました。
日本集中治療医学会「日本版重症患者の栄養療法ガイドライン」








コメント